Impfstoffe gegen Corona wurden in einer unglaublichen Geschwindigkeit entwickelt. CNN berichtet, dass die Entwickler bei Moderna bereits am 13. Januar 2020, zwei Tage nachdem die chinesischen Behörden die Gensequenz des Corona-Virus veröffentlichten den Impfstoff entwickelt hatten und anschließend mit der Herstellung von Impfdosen für klinische Tests begannen. Die Tests sollten schließlich noch mehrere Monate dauern, obwohl zur Beschleunigung die üblichen Testphasen parallel durchgeführt wurden.
Zeitintensiv ist besonders der Nachweis der Effektivität, also wie gut der Impfstoff schützt. Die bisher üblichen Verfahren setzen darauf, dass sich Studienteilnehmer zufällig auf natürliche Weise mit dem Virus infizieren. Die Effektivität könnte allerdings durch absichtliche Ansteckungen im Rahmen von sogenannten Human Challenge Trials deutlich schneller bestimmt werden. Das könnte angesichts zahlreicher Mutanten des Virus auch für die aktuelle Pandemie eine relevante Möglichkeit sein, wenn Zulassungsbehörden erneut Effektivitätsnachweise verlangen.
Beschleunigung für Corona
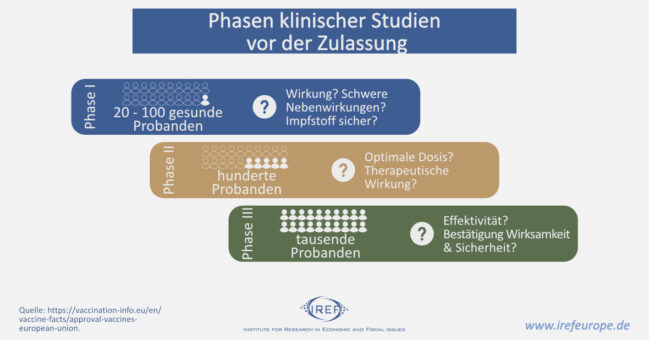
Neue Wirkstoffe durchlaufen bis zur Zulassung durch die Behörden verschiedene Überprüfungsphasen. Diese wurden für die Entwicklung der Corona-Impfstoffe nicht nacheinander durchgeführt, sondern parallel. So wurde Zeit gespart.
Bevor ein neuer Wirkstoff bei Menschen angewendet wird, werden zunächst Versuche in Laboren und schließlich an Tieren durchgeführt. Bei positiven Ergebnissen starten anschließend Versuche mit Menschen. Zunächst werden circa 20 bis 100 Probanden geringe Dosen des Wirkstoffs verabreicht, um erste Erkenntnisse über die Verträglichkeit zu gewinnen. Anschließend wird in Phase 2 der Kreis der Probanden auf mehrere Hundert ausgeweitet, um die therapeutische Wirkung zu überprüfen und die optimale Dosierung zu entwickeln.
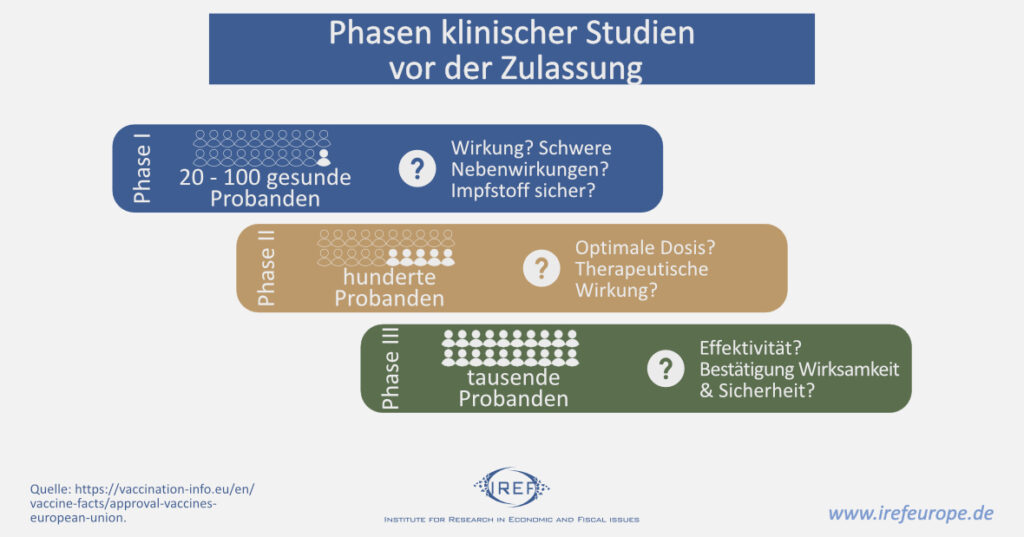
3. Phase: Tödliches Warten auf Infektionen
In der dritten Phase nehmen schließlich mehrere Tausend Probanden teil, um die Sicherheit des Wirkstoffes zu bestätigen und den Grad der Wirksamkeit zu ermitteln. Im Falle von Impfstoffen werden die Probanden zufällig in zwei Gruppen eingeteilt. Eine Gruppe erhält die tatsächliche Impfung und die zweite ein Placebo. Dann beginnt das große Warten. Es wird solange gewartet, bis sich in der Placebogruppe eine statistisch auswertbar hohe Anzahl an Probanden auf natürliche Weise mit der jeweiligen Krankheit infiziert.
In der Phase-3-Studie von BioNtech und Pfizer konnte die für die Zulassung relevante Auswertung erfolgen, nachdem sich von den 18.325 Probanden der Placebogruppe 162 infiziert hatten. In der gleichen Zeit hatten sich in der Gruppe der Geimpften von 18.198 Probanden lediglich 8 infiziert. Aus der relativen Häufigkeit der Erkrankungen in den beiden Gruppen wurde eine Effektivität von 95 Prozent abgeleitet.
Wohlgemerkt, das monatelange Warten auf natürliche Infektionen dient nicht dem Erkenntnisgewinn darüber, ob die Impfung sicher ist, also ob etwa unerwünschte Nebenwirkungen auftreten. Dafür verlangen die Zulassungsbehörden zunächst lediglich einen Beobachtungszeitraum von zwei Monaten nach der letzten Impfung. Es geht primär darum, die Effektivität zu überprüfen.
Während des Wartens auf die natürliche Infizierung der Testgruppen ging auch bei der Entwicklung der Corona-Impfstoffe wertvolle Zeit verloren. Viele Millionen Menschen außerhalb der Testgruppen infizierten sich während der Testphase mit dem Virus und starben.
Alternatives Verfahren: Human Challenge Trials
Um die Effektivität eines Impfstoffs nachzuweisen sind Phase-3-Studien mit der Beobachtung der natürlichen Ansteckung nicht alternativlos. Bei sogenannten Human Challenge Trials wird einer kleinen Gruppe junger gesunder Menschen der Impfstoff verabreicht. Anschließend werden die Probanden kontrolliert dem Virus ausgesetzt, um die Effektivität der Impfungen gegen das Corona-Virus zu ermitteln. Die Anzahl der Probanden kann dabei schrittweise erhöht werden, sodass nur bei zunehmender positiver Evidenz mehr Menschen der Gefahr einer Infektion ausgesetzt werden. Der Vorteil ist, dass nicht tausende Probanden geimpft werden müssen und auf eine natürliche Infizierung gewartet werden muss. So können Erkenntnisse über die Wirksamkeit deutlich schneller gewonnen werden. Ob diese Erkenntnisse auch auf ältere Personen übertragbar sind, ist unter Experten strittig.
Absichtliche Infizierung: Eine ethische Abwägung
Challenge Trials sind umstritten, da Menschen dem Virus absichtlich ausgesetzt werden. Bei der Abwägung sollte allerdings die Alternative berücksichtigt werden: Phase-3-Studien mit natürlicher Infizierung durch Abwarten und damit einhergehenden Erkrankungs- sowie Todesfällen durch den Zeitverlust.
Normalerweise werden Challenge Trials nur durchgeführt, wenn es für die Krankheit, gegen die ein Wirkstoff gesucht wird, eine rettende Therapie gibt. Die WHO hat zu Beginn der aktuellen Pandemie allerdings ihre Empfehlungen geändert und festgelegt, unter welchen Bedingungen das Verfahren auch für Corona möglich ist, obwohl es keine rettende Therapie gibt. So müssen die Freiwilligen etwa umfänglich über die Risiken informiert werden, die mit einer Teilnahme einhergehen. Das Risiko, welches die jungen Freiwilligen eingehen würden, wäre ähnlich hoch wie bei medizinischen Eingriffen, die vornehmlich anderen Menschen zugutekommen, wie etwa Organspenden.
Nichts Neues und in Planung
Human Challenge Trials sind in der Erforschung von Medikamenten nichts Neues. So wurden sie bereits für die Entwicklung von Impfstoffen gegen Pocken, Influenza, Cholera und Typhuseingesetzt.
Die britische Regierung bereitet derzeit zusammen mit dem Imperial College London Challenge Trials für Corona-Impfstoffe vor. Bisher ist nicht bekannt, welche Impfstoffproduzenten auf dieses Verfahren zurückgreifen werden. Inzwischen haben sich allerdings bereits über 38.000 Menschen als Freiwillige für mögliche Challenge Trials auf der Seiter der Initiative 1daysooner gemeldet.
Auch jetzt können Challenge Trials noch einen Unterschied machen
Auch wenn es inzwischen erste zugelassene Impfstoffe gibt. Das Problem des Wartens auf Ergebnisse aus Phase-3-Studien besteht weiter: Nämlich für die Impfstoffe, die bereits entwickelt wurden und derzeit getestet werden und etwaige weitere Impfstoffe, die noch entwickelt werden – möglicherweise auch in Reaktion auf neue Mutationen des Virus. Im Zuge der Coronabekämpfung gemachte Erfahrungen, könnten zudem wertvoll für den Umgang mit zukünftigen Pandemien sein.
Die Testung von neuen Wirkstoffen ist immer ein ethisches Dilemma. Auf der einen Seite schrecken wir intuitiv davor zurück, selbst gesunde junge Menschen absichtlich einer Gefahr auszusetzten. Doch die Alternative ist nicht weniger problematisch. Ein monatelanger Verzug in der Testphase kann zu vielen Toten führen, wie die Corona-Pandemie zeigt. Für die Entwicklung und Weiterentwicklung von Impfstoffen gegen Corona sollten Challenge Trials zur Beschleunigung kein Tabu sein. Sie können Menschenleben retten und wurden bereits in der Vergangenheit vielfach erfolgreich eingesetzt.
Erschienen bei: IREF. Mitautor: Dr. Alexander Fink.